Tras una fractura, el hueso y los tejidos circundantes sufren daños, y existen diferentes principios y métodos de tratamiento según el grado de la lesión. Antes de tratar cualquier fractura, es fundamental determinar la extensión de la lesión.
Lesiones de tejidos blandos
I. Clasificación
Fracturas cerradas
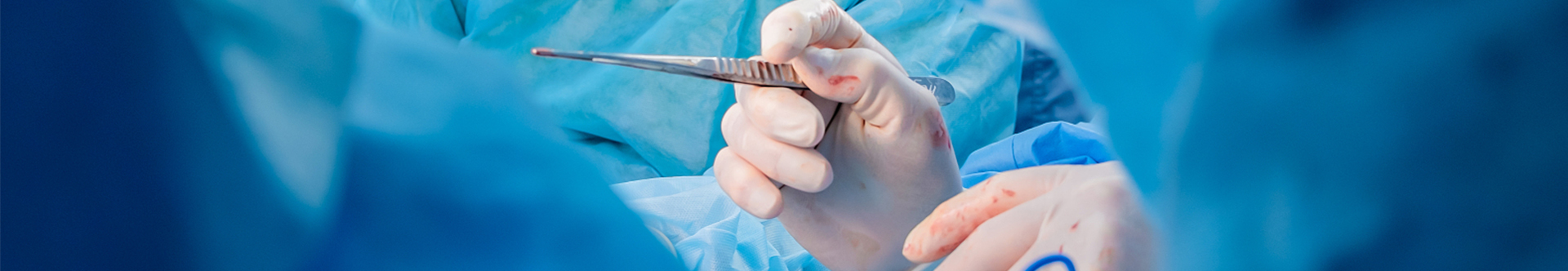
Las lesiones de tejidos blandos se clasifican de leves a graves, generalmente utilizando el método de Tscherne (Fig. 1).
Lesión de grado 0: lesión menor de tejidos blandos
Lesión de grado 1: abrasión superficial o contusión del tejido blando que cubre el sitio de la fractura.
Lesión de grado 2: contusión muscular significativa o contusión cutánea contaminada o ambas
Lesión de grado 3: lesión grave de tejidos blandos con desplazamiento grave, aplastamiento, síndrome compartimental o lesión vascular.
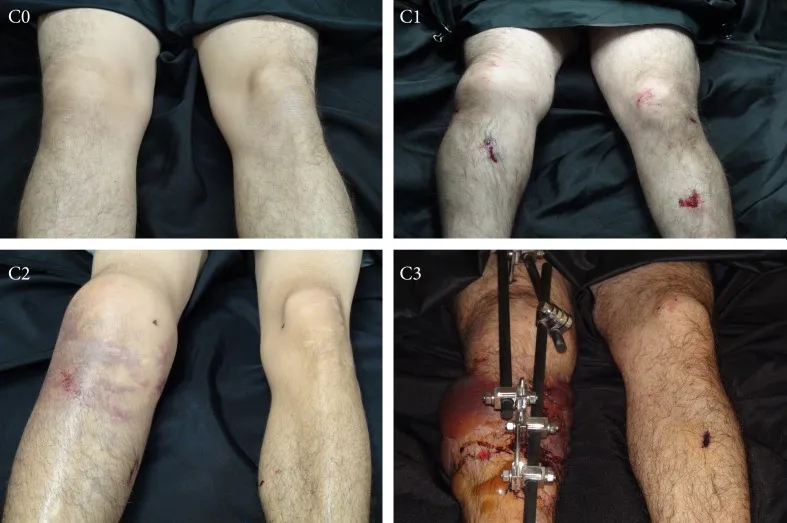
Figura 1: Clasificación de Tscherne
Fractura abierta
Debido a que la fractura es comunicativa al mundo exterior, el grado de daño de los tejidos blandos está relacionado con la cantidad de energía experimentada por la extremidad durante el trauma, y generalmente se utiliza la clasificación de Gustilo (Figura 2).
Figura 2: Clasificación de Gustilo
Tipo I: longitud de herida limpia < 1 cm, daño muscular leve, sin exfoliación perióstica evidente. Tipo II: longitud de herida > 1 cm, sin daño evidente de tejidos blandos, formación de colgajo o lesión por avulsión.
Tipo III: El rango de heridas incluye piel, músculo, periostio y hueso, con traumatismos más extensos, incluidos tipos especiales de heridas de bala y lesiones agrícolas.
Tipo IIIa: Contaminación generalizada y/o presencia de lesiones profundas de tejidos blandos, tejidos blandos con cobertura adecuada de estructuras óseas y neurovasculares.
Tipo IIIb: con daño extenso de tejidos blandos, se requieren metástasis musculares rotacionales o libres durante el tratamiento para lograr la cobertura.
Tipo IIIc: Fracturas abiertas con daño vascular que requieren reparación manual. La clasificación de Gustilo tiende a empeorar progresivamente con el tiempo y se observan cambios en el grado de lesión durante la reparación.
II. Manejo de lesiones
La cicatrización de heridas requiere oxigenación, activación de los mecanismos celulares y limpieza de las heridas para eliminar el tejido contaminado y necrótico. Existen cuatro etapas principales de cicatrización: coagulación (minutos); fase inflamatoria (horas); fase de tejido de granulación (días); y período de formación de tejido cicatricial (semanas).
Estadificación del tratamiento
Fase aguda:irrigación de heridas, desbridamiento, reconstrucción ósea y recuperación del rango de movimiento
(1) Evaluar la extensión de la lesión de tejidos blandos y la lesión neurovascular relacionada.
(2) Utilice una gran cantidad de líquido isotónico para irrigación pulsátil en el quirófano para eliminar tejido necrótico y cuerpos extraños.
(3) El desbridamiento se realiza cada 24 a 48 horas para eliminar todos los cuerpos extraños y tejidos necróticos de la herida hasta que la herida pueda cerrarse o cubrirse por completo. (4) La herida abierta se extiende adecuadamente, el tejido profundo se expone completamente y se llevan a cabo una evaluación y un desbridamiento efectivos.
(5) El extremo libre de la fractura se retrae dentro de la herida; se retira una pequeña corteza desactivada para examinar y limpiar la cavidad de la médula ósea.
Reconstrucción:Tratamiento de las secuelas del trauma (retraso en la unión, falta de unión, deformidad, infección)
Convalecencia:Regresión psicológica, social y ocupacional del paciente
Tipo de cierre y cobertura de la herida
El cierre o cobertura temprana de la herida (3 a 5 días) puede lograr resultados satisfactorios del tratamiento: (1) cierre primario
(2)cierre retrasado
(3)cierre secundario
(4) Trasplante de colgajo de grosor medio
(5)colgajo voluntario (colgajo digital adyacente)
(6) colgajo de pedículo vascular (colgajo de gastrocnemio)
(7) colgajo libre (Fig. 3)
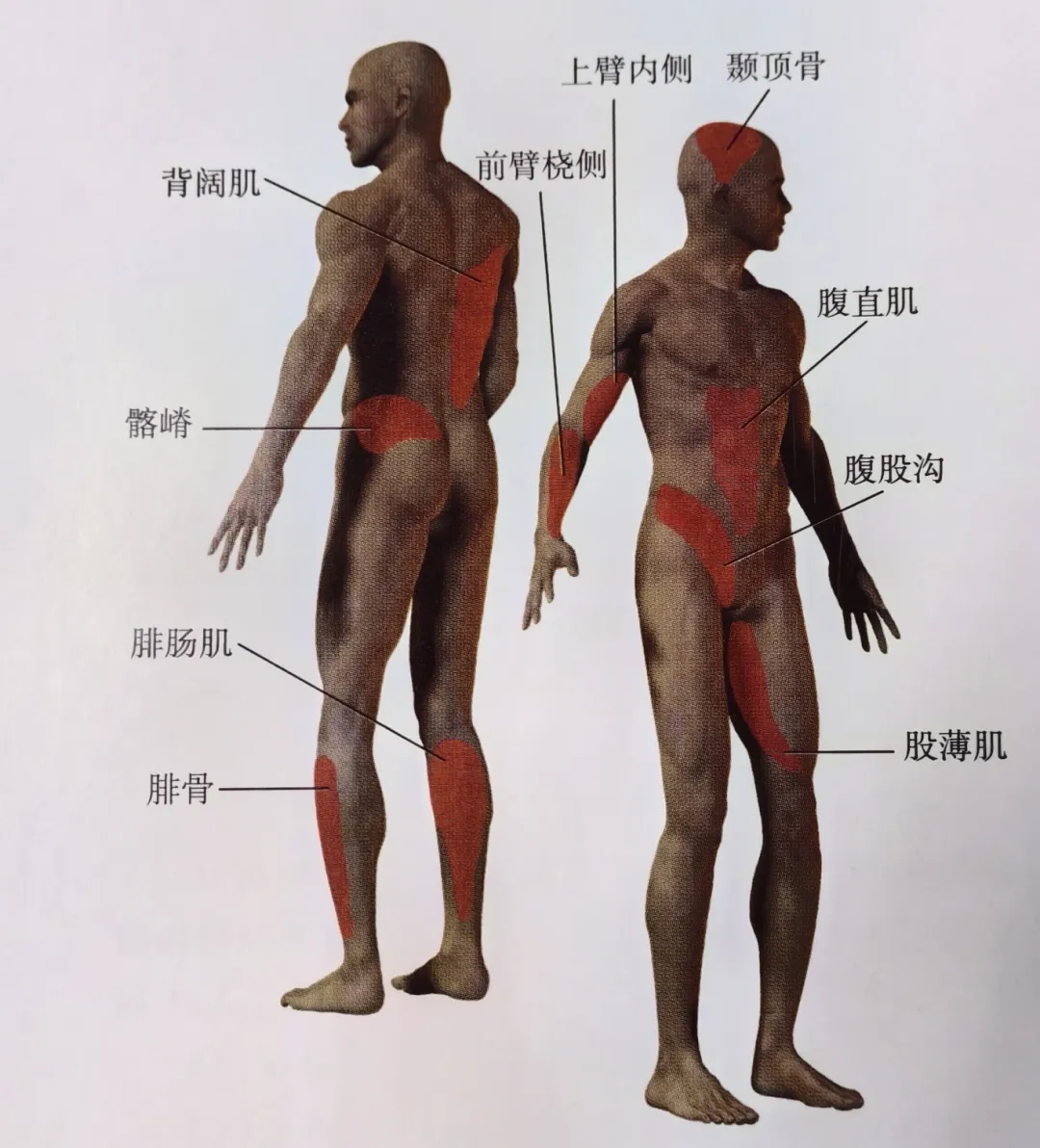
Figura 3: A menudo se proporcionan vistas parciales de trasplantes libres.
Daño óseo
I.Dirección de la línea de fractura
Transversal: Patrón de carga de una fractura transversal causada por tensión
oblicuamente: Modo de carga de una presión debido a una fractura diagonal
Espiral: Patrón de carga de una fractura torsional debido a una fractura espiral
II. Fracturas
Clasificación según fracturas, tipos de fractura, etc. (Fig. 4)
Las fracturas conminutas son fracturas con 3 o más fragmentos óseos vivos, generalmente resultado de una lesión de alta energía.
La fractura patológica de la línea de fractura se produce en la zona de deterioro óseo de la enfermedad previa, incluyendo: tumor óseo primario, metástasis óseas, osteoporosis, enfermedad ósea metabólica, etc.
Las fracturas incompletas no se rompen en fragmentos separados de hueso.
Fracturas segmentarias con fragmentos distales, medios y proximales. El segmento medio se ve afectado por el riego sanguíneo, generalmente como resultado de una lesión de alta energía, con desprendimiento de tejido blando del hueso, lo que dificulta la consolidación ósea.
Fracturas con defectos óseos, fracturas abiertas con fragmentos óseos o fracturas inactivas por traumatismo que necesitan ser limpiadas, o fracturas conminutas graves que resultan en defectos óseos.
Las fracturas con fragmentos de hueso en mariposa son similares a las fracturas segmentarias en que no afectan toda la sección transversal del hueso y generalmente son el resultado de una flexión violenta.
Las fracturas por estrés son causadas por cargas repetidas y a menudo ocurren en el calcáneo y la tibia.
Las fracturas por avulsión provocan una fractura del punto de inserción del hueso cuando se estira un tendón o ligamento.
Las fracturas por compresión son fracturas en las que los fragmentos óseos se comprimen, generalmente por cargas axiales.
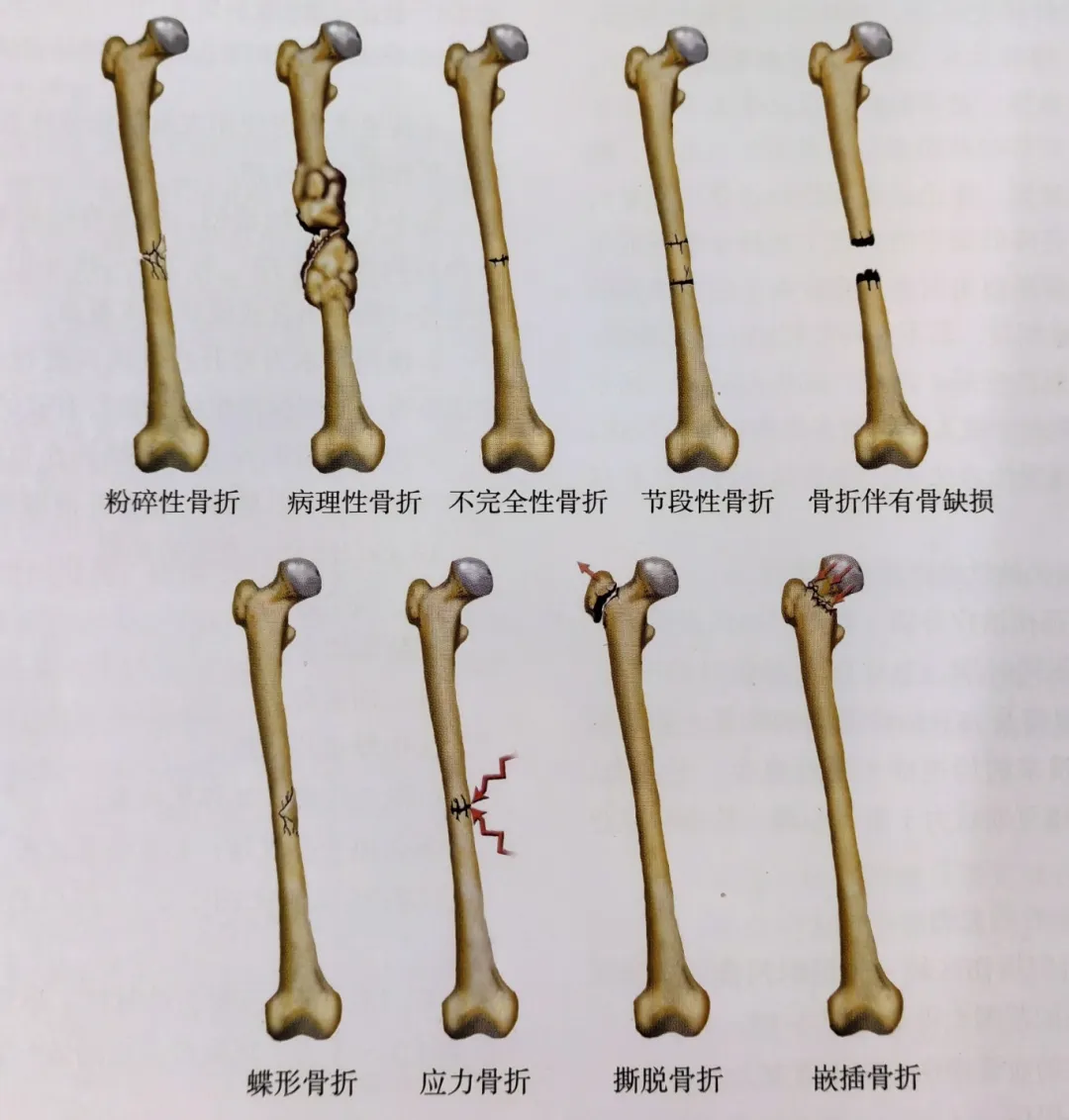
Figura 4: Clasificación de las fracturas
III. Factores que influyen en la consolidación de fracturas
Factores biológicos: edad, enfermedad ósea metabólica, enfermedad de base, nivel funcional, estado nutricional, función neurológica, daño vascular, hormonas, factores de crecimiento, estado de salud de la cápsula de tejido blando, grado de esterilidad (fractura abierta), tabaquismo, medicación, patología local, nivel de energía traumática, tipo de hueso, grado de defecto óseo, factores mecánicos, grado de unión del tejido blando al hueso, estabilidad, estructura anatómica, nivel de energía traumática, grado de defecto óseo.
IV. Modalidades de tratamiento
El tratamiento no quirúrgico está indicado en pacientes con lesiones de baja energía o inoperables por factores sistémicos o locales.
Reductor: tracción a lo largo del eje largo de la extremidad, separación de la fractura.
Fijación con férula en ambos extremos de la fractura nuevamente: fijación del hueso reducido mediante fijación externa, incluyendo la técnica de fijación de tres puntos.
Técnica de fijación por compresión continua del hueso tubular mediante tracción: una forma de reducción, que incluye tracción de la piel, tracción ósea.
Tratamiento quirúrgico
(1) La fijación externa es adecuada para fracturas abiertas, fracturas cerradas con traumatismo grave de tejidos blandos y fracturas acompañadas de infección (Fig. 5).
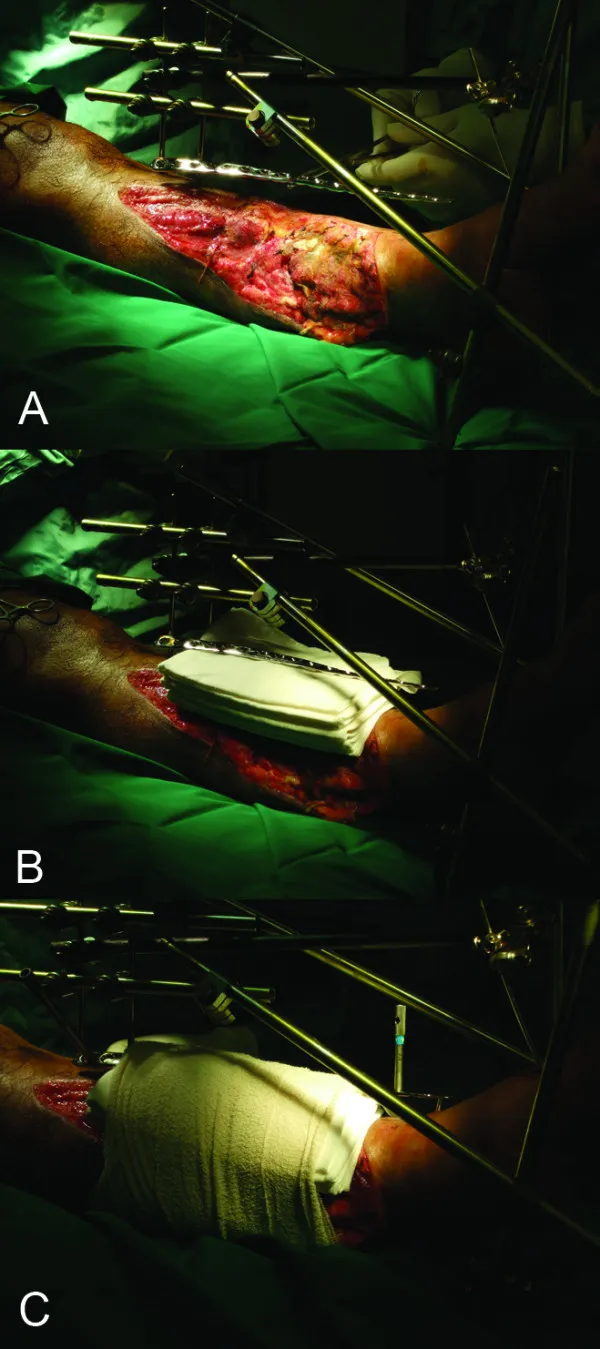
Figura 5: Procedimiento de fijación externa
(2) La fijación interna es aplicable a otros tipos de fracturas y sigue el principio AO (Tabla 1)

Tabla 1: Evolución de la AO en la terapia de fracturas
Los fragmentos entre fracturas requieren fijación por compresión, que incluye compresión estática (tornillos de compresión), compresión dinámica (clavos intramedulares sin bloqueo), entablillado (deslizamiento entre el objeto interno y el hueso) y fijación de puente (material interno que abarca el área conminutada).
(4)Reducción indirecta:
La tecnología de tracción se implementa en el área conminuta de la fractura para reducir el fragmento a través de la tensión del tejido blando, y la fuerza de tracción se deriva del dispositivo de tracción femoral, el fijador externo, el dispositivo de tensión de la articulación AO o el abridor de lámina.
V.Estadificación del tratamiento
Según el proceso bioquímico de consolidación de la fractura, este se divide en cuatro etapas (Tabla 2). A su vez, en combinación con el proceso bioquímico, el tratamiento de la fractura se divide en tres etapas, lo que promueve la finalización del proceso bioquímico y la consolidación de la fractura (Fig. 6).

Tabla 2: Curso de vida de la curación de fracturas
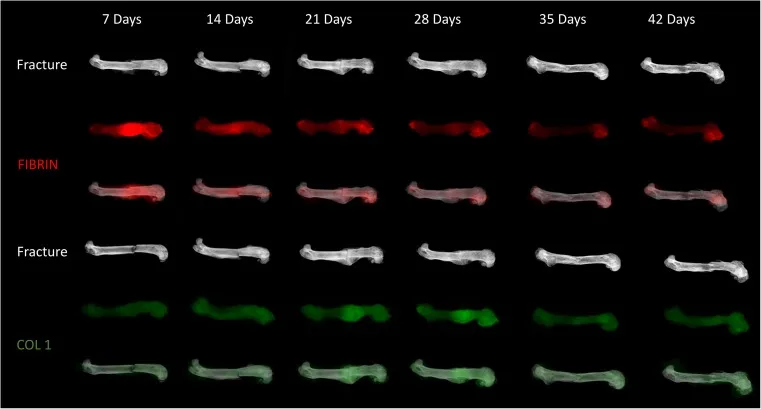
Figura 6: Diagrama esquemático de la curación de fracturas en ratones
Fase inflamatoria
La hemorragia del sitio de la fractura y los tejidos blandos circundantes forma un hematoma, se forma tejido fibrovascular en el extremo fracturado y los osteoblastos y fibroblastos comienzan a proliferar.
Falta del tiempo
La respuesta original del callo ocurre dentro de las 2 semanas, con la formación de un esqueleto de cartílago seguido de la formación de un callo a través de la osificación endocondral, y todas las formas específicas de curación de la fractura están relacionadas con la modalidad de tratamiento.
Reconstrucción
Durante el proceso de reparación, el hueso trenzado formado se reemplaza por hueso laminar y se recanaliza la cavidad medular para marcar la finalización de la reparación de la fractura.
Complicación
La unión retardada se manifiesta principalmente porque la fractura no se cura dentro del tiempo esperado, pero aún tiene cierta actividad biológica, y las razones para la unión retardada son variadas y están relacionadas con los factores que afectan la curación de la fractura.
La pseudoartrosis se manifiesta como una fractura sin evidencia de curación clínica ni radiológica y las principales manifestaciones son:
(1)Pseudoartrosis atrófica debida a la falta de vascularización y a la falta de capacidad biológica para sanar, que generalmente se manifiesta como estenosis del extremo roto del hueso y ausencia de vasos sanguíneos, y el proceso de tratamiento requiere estimulación de la actividad biológica local (injerto óseo o resección cortical ósea y transporte óseo).
(2)La pseudoartrosis hipertrófica tiene vascularización transicional y capacidad biológica, pero carece de estabilidad mecánica, lo que generalmente se manifiesta como un crecimiento excesivo del extremo roto de la fractura, y el tratamiento debe aumentar la estabilidad mecánica (fijación con placa ósea y tornillos).
(3) La pseudoartrosis distrófica tiene suficiente suministro de sangre, pero casi no hay formación de callo y es necesario volver a realizar la reducción de la fractura debido al desplazamiento y la reducción insuficientes del extremo roto de la fractura.
(4) En caso de pseudoartrosis infecciosa con infección crónica, el tratamiento debe primero eliminar el foco infeccioso y luego promover la consolidación de la fractura. La osteomielitis infecciosa ósea es una enfermedad ósea e infecciosa, que puede ser una infección directa de heridas abiertas o una infección patógena por vía hemática. Es necesario identificar los microorganismos y patógenos infectados antes del tratamiento.
El síndrome de dolor regional complejo se caracteriza por dolor, hiperestesia, alergias en las extremidades, flujo sanguíneo local irregular, sudoración y edema, incluyendo anomalías del sistema nervioso autónomo. Suele presentarse tras un traumatismo o una cirugía, y se detecta y trata precozmente, con bloqueo simpático si es necesario.
• La osificación heterotópica (HO) es común después de un traumatismo o una cirugía, y es más común en el codo, la cadera y el muslo, y los bifosfonatos orales pueden inhibir la mineralización ósea después del inicio de los síntomas.
• La presión en el compartimento perifisal aumenta hasta un cierto nivel, lo que perjudica la perfusión interna.
• La lesión neurovascular tiene diferentes causas debido a diferentes ubicaciones anatómicas.
• La necrosis avascular se produce en zonas con suministro de sangre insuficiente, véase específicamente la lesión y la localización anatómica, etc., y se produce un daño irreversible.
Hora de publicación: 31 de diciembre de 2024